Υπερβολικοί ισχυρισμοί σχετικά με το ρωσικό εμβόλιο κατά του καρκίνου Enteromix διαδίδονται στην Ελλάδα
- Δημοσιεύθηκε στις 9 Οκτωβρίου 2025 στις 10:51
- 7 λεπτά ανάγνωσης
- Του/Της: Tolera FIKRU GEMTA, AFP Αιθιοπία
- Μετάφραση και προσαρμογή Magdalini GKOGKOU, AFP Ελλάδα
«Έτοιμο για χρήση το Ρωσικό εμβόλιο, κατά του καρκίνου και περιμένει την επίσημη έγκρισή του», αναφέρει αυτή η μακροσκελής ανάρτηση στο Facebook, η οποία έχει κοινοποιηθεί περισσότερες από 50 φορές. Παραποιώντας τα λόγια της Βερόνικα Σκβόρτσοβα, επικεφαλής της Ομοσπονδιακής Ιατρικής και Βιολογικής Υπηρεσίας της Ρωσίας, σε συνέντευξη που έδωσε στο ρωσικό μέσο ενημέρωσης Izvestia στις 5 Σεπτεμβρίου, η ανάρτηση συνεχίζει αναφέροντας ότι οι κλινικές δοκιμές του εμβολίου Enteromix κατά του καρκίνου έχουν ολοκληρωθεί, αποδεικνύοντας την «ασφάλεια και την υψηλή αποτελεσματικότητά» του.
Στην πραγματικότητα, χωρίς να κατονομάσει το εμβόλιο, η Σκβόρτσοβα δήλωσε στο Izvestia ότι «ένα ρωσικό εμβόλιο» είχε ολοκληρώσει με επιτυχία τις προκλινικές δοκιμές και ότι στα τέλη του καλοκαιριού του 2025 είχαν υποβληθεί έγγραφα στις αρχές για την έγκριση της κλινικής χρήσης του νέου φαρμάκου. Οι προκλινικές δοκιμές αφορούν οποιαδήποτε έρευνα περιλαμβάνει πειράματα και δοκιμές σε ζώα για να αξιολογηθεί το δυναμικό μιας θεραπείας, χωρίς όμως να προβλέπουν την αντίδραση του ανθρώπινου οργανισμού.
Ενώ ορισμένα ρωσικά μέσα ενημέρωσης ισχυρίζονται ότι η Σκβόρτσοβα αναφέρεται στο Enteromix (παραδείγματα εδώ και εδώ), το AFP δεν βρήκε καμία αναφορά στο συγκεκριμένο εμβόλιο στη συνέντευξή της.
Ο ιστότοπος του Εθνικού Ιατρικού Ερευνητικού Ραδιολογικού Κέντρου της Ρωσίας (NMRRC) περιγράφει το Enteromix ως φάρμακο που βασίζεται σε έναν συνδυασμό τεσσάρων μη παθογόνων ιών, σχεδιασμένο να στοχεύει κακοήθη κύτταρα και να ενεργοποιεί την αντικαρκινική ανοσία του ασθενούς. Παράλληλα, τα «εξατομικευμένα» εμβόλια mRNA, προσαρμοσμένα στον καρκίνο κάθε ατόμου, αναπτύσσονται για να «διδάσκουν» το ανοσοποιητικό σύστημα του ασθενούς να στοχεύει και να εξαλείφει τα καρκινικά κύτταρα, σύμφωνα με τον ιστότοπο.
Παρόμοιοι παραπλανητικοί ισχυρισμοί που εξυμνούν τα υποτιθέμενα οφέλη του Enteromix, κυκλοφόρησαν από άλλους χρήστες στο Facebook (εδώ, εδώ και εδώ).
Άλλοι ισχυρισμοί σχετικά με το εμβόλιο κατά του καρκίνου διαδόθηκαν στα αγγλικά σε διάφορες αφρικανικές χώρες, μεταξύ άλλων στο Καμερούν και τη Νότια Αφρική, καθώς και στα αμχαρικά, μία από τις δύο κύριες γλώσσες της Αιθιοπίας.
Έτοιμο για την αγορά;
Δεν υπάρχουν στοιχεία που να αποδεικνύουν ότι το Enteromix έχει κυκλοφορήσει στο κοινό, πόσο μάλλον ότι έχει εγκριθεί για γενική χρήση, είτε στη Ρωσία είτε οπουδήποτε αλλού στον κόσμο.
Ωστόσο, η δημιουργία ενός ακριβούς χρονοδιαγράμματος που να καλύπτει την ακριβή εξέλιξη του Enteromix και άλλων ρωσικών εμβολίων κατά του καρκίνου είναι περίπλοκη λόγω των διάφορων δηλώσεων που περιλαμβάνονται σε αναφορές που βρήκε η ομάδα επαλήθευσης γεγονότων του AFP στο διαδίκτυο.
Τρεις μήνες πριν από τη συνέντευξη της Σκβόρτσοβα, το ρωσικό Υπουργείο Υγείας είχε ανακοινώσει ότι ειδικοί είχαν ξεκινήσει κλινικές δοκιμές του Enteromix -- τον Ιούνιο του 2025, με τη συμμετοχή 48 εθελοντών.
Ο Αντρέι Καπρίν, επικεφαλής ογκολόγος του υπουργείου και γενικός διευθυντής του NMRRC, περιέγραψε τη μελέτη ως «ανοιχτή, μονοκεντρική κλινική δοκιμή φάσης Ι».
Το κέντρο που διευθύνει ο Καπρίν ανακοίνωσε στον ιστότοπό του ότι «ολοκληρώθηκε ένας πλήρης κύκλος προκλινικών μελετών» τα «τελευταία χρόνια», προσθέτοντας ότι «είναι σημαντικό να σημειωθεί ότι οι κλινικές δοκιμές και η πρόσληψη ασθενών για την πρώτη φάση θα ξεκινήσουν στα τέλη του 2024, αρχές του 2025».
Ειδικοί επιβεβαίωσαν ότι απαιτούνται συγκεκριμένα κλινικά στοιχεία προτού το εμβόλιο εγκριθεί για γενική χρήση.

Μια αυστηρή διαδικασία
Σύμφωνα με τον Δρ. Λέναρντ Λι, καθηγητή στο Πανεπιστήμιο της Οξφόρδης και σύμβουλο στην ιατρική ογκολογία, η ανάπτυξη και η έγκριση των εμβολίων ακολουθούν μια σαφώς καθορισμένη ακολουθία. Σε απαντήσεις μέσω μηνύματος ηλεκτρονικού ταχυδρομείου προς το AFP στις 16 και 22 Σεπτεμβρίου 2025, ο ειδικός εξήγησε ότι η διαδικασία ξεκινά με προκλινικές μελέτες σε εργαστήριο και τη χρήση ζωικών μοντέλων για την αξιολόγηση της ανοσολογικής απόκρισης και της βασικής ασφάλειας. Οι προκλινικές δοκιμές ακολουθούνται από ιατρικές δοκιμές με στόχο την αξιολόγηση του δυναμικού μιας θεραπείας σε ανθρώπους, συνήθως σε τρεις φάσεις.
Οι δοκιμές φάσης Ι σε ανθρώπους ελέγχουν την ασφάλεια και τη δοσολογία σε μικρές ομάδες ασθενών, είπε ο Λι, και ακολουθούν δοκιμές φάσης ΙΙ σε μεγαλύτερες ομάδες για την αναζήτηση πρώιμων ενδείξεων κλινικού οφέλους, ενώ συνεχίζεται η παρακολούθηση της ασφάλειας. Οι δοκιμές φάσης ΙΙΙ περιλαμβάνουν μεγάλες, ελεγχόμενες μελέτες για την επιβεβαίωση της αποτελεσματικότητας του εμβολίου σε δείκτες όπως τα ποσοστά υποτροπής, η επιβίωση χωρίς εξέλιξη της νόσου ή η συνολική επιβίωση. Αυτή η διαδικασία μπορεί να διαρκέσει έως και 10 χρόνια -- ή και περισσότερο.
Παράλληλα, οι ρυθμιστικές αρχές αξιολογούν την ποιότητα της παραγωγής, τη συνέπεια και την παρακολούθηση της ασφάλειας. Μόνο μέσω αυτής της προσεκτικής, σταδιακής διαδικασίας μπορεί να εδραιωθεί η εμπιστοσύνη ότι ένα εμβόλιο κατά του καρκίνου είναι πραγματικά ασφαλές και αποτελεσματικό, δήλωσε ο Λι.
Η διαδικασία που περιγράφεται από τον Λι εξηγείται περαιτέρω σε άρθρο του Εθνικού Κέντρου Έρευνας και Παρακολούθησης Ανοσοποίησης (NCIRS) της Αυστραλίας.
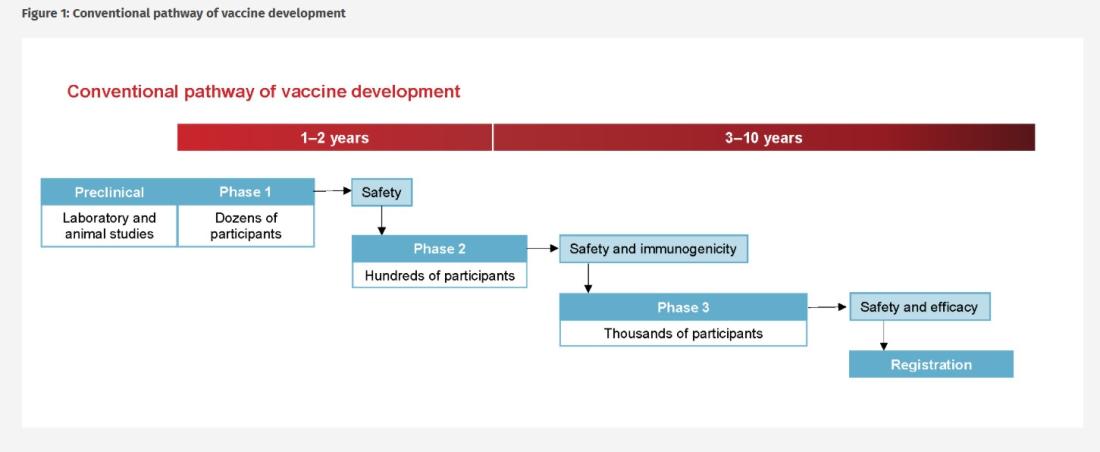
Διαφανή δεδομένα, τεκμηριωμένα στοιχεία που έχουν αξιολογηθεί από ομότιμους και αυστηρά πρότυπα παραγωγής είναι επίσης απαραίτητα. «Χωρίς αυτά, οι ασθενείς και οι κλινικοί γιατροί θα δυσκολευτούν να χτίσουν την εμπιστοσύνη που είναι απαραίτητη στη θεραπεία του καρκίνου», δήλωσε ο Λι στο AFP.
Ο Δρ Πάτρικ Οττ, καθηγητής της Ιατρικής Σχολής του Χάρβαρντ και κλινικός διευθυντής του Ινστιτούτου Καρκίνου Ντάνα Φάρμπερ (DFCI), δήλωσε στο AFP μέσω συνέντευξης στο Zoom στις 17 Σεπτεμβρίου 2025 ότι τα συστήματα ρύθμισης των εμβολίων μπορεί να διαφέρουν σε όλο τον κόσμο και δεν είναι όλα εξίσου αυστηρά.
«Ανεξάρτητα από το ρυθμιστικό σύστημα, τα δεδομένα των κλινικών δοκιμών είναι απαραίτητα για να τεκμηριώσουν τους ισχυρισμούς ότι ένα εμβόλιο είναι ασφαλές και αποτελεσματικό για γενική χρήση», είπε.
Ο Λι εξήγησε γιατί απαιτούνται συγκεκριμένα κλινικά στοιχεία προτού το εμβόλιο εγκριθεί για γενική χρήση.
«Η εγγραφή μόνο 48 συμμετεχόντων θεωρείται γενικά μια πολύ μικρή μελέτη σε πρώιμο στάδιο -- πιο κοντά σε δοκιμή Φάσης Ι ή εξερευνητική δοκιμή Φάσης ΙΙ», είπε.
Ο Λι πρόσθεσε ότι μια μελέτη Φάσης ΙΙΙ, η οποία συνήθως περιλαμβάνει εκατοντάδες έως χιλιάδες ασθενείς, είναι απαραίτητη για τη δημιουργία αξιόπιστων δεδομένων σχετικά με την ασφάλεια, την αποτελεσματικότητα και τη διάρκεια των οφελών.
«Δεν μπορώ να βρω καμία επιστημονική απόδειξη που να έχει αξιολογηθεί από ομότιμους ότι αυτό το εμβόλιο Enteromix έχει δοκιμαστεί σε κλινικές δοκιμές σε ανθρώπους», είπε.
«Για μια θεραπεία τόσο σημαντική όσο ένα εμβόλιο κατά του καρκίνου πρέπει να υπάρχουν ορατά στοιχεία και διαφάνεια».
Πλήρης αποτελεσματικότητα;
Ακόμη και οι πιο αισιόδοξες δηλώσεις από Ρώσους αξιωματούχους δεν περιγράφουν το Enteromix ως «μαγική λύση» για τον καρκίνο, παρά τον ισχυρισμό ότι το εμβόλιο έδειξε «100%» αποτελεσματικότητα στην εξάλειψη των καρκινικών κυττάρων κατά τη διάρκεια των δοκιμών.
Στην συνέντευξή της στην Izvestia, η Σκβόρτσοβα δήλωσε ότι το εμβόλιο εστιάζει κυρίως στον καρκίνο του παχέος εντέρου και ενδέχεται τελικά να επεκταθεί για τη θεραπεία δύο άλλων τύπων καρκίνου -- του γλοιοβλαστώματος, ενός από τους πιο κακοήθεις όγκους του εγκεφάλου, και ειδικών τύπων μελανώματος, ενός καρκίνου του δέρματος.
Η Σκβόρτσοβα πρόσθεσε ότι οι προκλινικές δοκιμές «απέδειξαν την ασφάλεια του εμβολίου» και «την υψηλή αποτελεσματικότητά του στη μείωση του μεγέθους των όγκων και στην επιβράδυνση της ανάπτυξής τους κατά 60-80%».
Σε συνέντευξη που παραχώρησε στον ρωσικό όμιλο μέσων ενημέρωσης RBC τον Ιούνιο του 2024, ο Βιατσεσλάβ Κοσορούκοφ, διευθυντής του Ερευνητικού Ινστιτούτου Πειραματικής Διαγνωστικής και Θεραπείας Όγκων στο Εθνικό Ιατρικό Ερευνητικό Κέντρο Ογκολογίας N.N. Μπλόκιν, δήλωσε σχετικά με το έργο τους για την ανάπτυξη ενός εμβολίου κατά του καρκίνου: «Η τεχνολογία που συζητάμε είναι πρωτοποριακή, αλλά δεν αποτελεί πανάκεια, ένα "χρυσό χάπι" για όλους τους τύπους καρκίνου».
Ο Οττ δήλωσε ότι οι ισχυρισμοί για πλήρη αποτελεσματικότητα απέχουν πολύ από την πραγματικότητα. «Δεν υπάρχει επί του παρόντος καμία θεραπεία για τον καρκίνο που να προσφέρει 100% ίαση», είπε, προσθέτοντας ότι «ο όρος "ίαση" είναι συχνά ασαφής, καθώς πολλοί καρκίνοι παραμένουν ανίατοι. Ο ισχυρισμός ότι ένα εμβόλιο θεραπεύει πλήρως τον καρκίνο είναι απλά απίστευτος».
Σε ερώτηση σχετικά με το Enteromix, ο Παγκόσμιος Οργανισμός Υγείας (ΠΟΥ) απάντησε μέσω μηνύματος ηλεκτρονικού ταχυδρομείου στο AFP στις 18 Σεπτεμβρίου 2025: «Ο ΠΟΥ δεν έχει καμία επίσημη συνεργασία με το πρόγραμμα».
Ο ΠΟΥ διευκρίνισε ότι οι εθνικές ή περιφερειακές ρυθμιστικές αρχές είναι υπεύθυνες για την έγκριση των εμβολίων, ενώ ο ρόλος του περιορίζεται κυρίως στην παροχή υποστήριξης για την προεπιλογή.
Το εμβόλιο mRNA-4157
Σύμφωνα με την Αμερικανική Εθνική Ιατρική Βιβλιοθήκη, η ανάπτυξη εμβολίων mRNA αποτελεί σημαντική πρόοδο στη θεραπεία του καρκίνου, με περισσότερες από 120 κλινικές δοκιμές μέχρι σήμερα να αποδεικνύουν το δυναμικό τους σε διάφορες κακοήθειες, όπως ο καρκίνος του πνεύμονα, του μαστού, του προστάτη, το μελάνωμα και πιο δύσκολες μορφές καρκίνου, όπως όγκοι του παγκρέατος και του εγκεφάλου.
Ενώ στη Ρωσία βρίσκονται σε φάση ανάπτυξης διάφορα εξατομικευμένα εμβόλια mRNA κατά του καρκίνου, σύμφωνα με αξιωματούχους και επιστήμονες, το υποψήφιο εμβόλιο mRNA-4157 κατά του καρκίνου, που αναπτύχθηκε από τις εταιρείες Moderna και Merck, έχει σημειώσει σημαντική πρόοδο στην κλινική ανάπτυξη και έχει χαρακτηριστεί «επαναστατικό» για τους ασθενείς με καρκίνο.
Το mRNA-4157 στοχεύει το μελάνωμα, έναν σοβαρό τύπο καρκίνου του δέρματος.
Το εμβόλιο βρίσκεται τώρα στη Φάση III της ανάπτυξής του, με τη συμμετοχή περισσότερων από 1.000 ατόμων σε δοκιμές σε όλο τον κόσμο, με σκοπό την επιβεβαίωση της αποτελεσματικότητάς του και την τελική έγκριση από τις ρυθμιστικές αρχές. Αν και το mRNA-4157 έχει λάβει τον τίτλο «FDA Breakthrough Therapy» (Πρωτοποριακή Θεραπεία του Οργανισμού Τροφίμων και Φαρμάκων των ΗΠΑ), εξακολουθεί να βρίσκεται υπό έρευνα.
Ο FDA απονέμει τον χαρακτηρισμό «Πρωτοποριακή Θεραπεία» για να επιταχύνει την ανάπτυξη θεραπειών για σοβαρές παθήσεις, όταν τα πρώτα στοιχεία υποδηλώνουν ότι αυτές μπορεί να προσφέρουν σημαντική βελτίωση σε σχέση με τις υπάρχουσες θεραπείες.
Οι δοκιμαστικές διαδικασίες για το mRNA-4157 έχουν διαρκέσει πάνω από έξι χρόνια και το εμβόλιο δεν έχει ακόμη κυκλοφορήσει στην αγορά.
Μια έκθεση του ΠΟΥ του Φεβρουαρίου 2025 αναφέρει ότι ο καρκίνος προκάλεσε σχεδόν 10 εκατομμύρια θανάτους το 2020, περίπου έναν στους έξι παγκοσμίως. Οι πιο συνηθισμένοι τύποι περιλαμβάνουν τον καρκίνο του μαστού, του πνεύμονα, του παχέος εντέρου και του προστάτη.
Το AFP έχει ήδη διαψεύσει και άλλους παραπλανητικούς ή ψευδείς ισχυρισμούς σχετικά με τα εμβόλια εδώ.
Πνευματικά δικαιώματα © AFP 2017-2026. Οποιαδήποτε εμπορική χρήση αυτού του περιεχομένου απαιτεί συνδρομή. Κάντε κλικ εδώ για να μάθετε περισσότερα.
Υπάρχει περιεχόμενο που θα θέλατε να ελέγξει το AFP;
Επικοινωνήστε μαζί μας